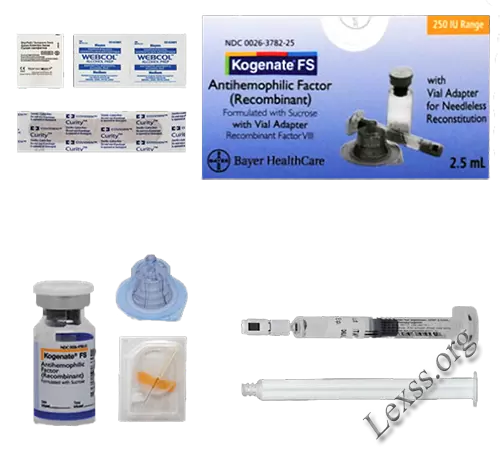
Когенейт ФС (Kogenate FS) – фактор згортання крові VIII
Виробник:
BAYER HealthCare LLC
Клініко-фармакологічна група:
Препарат фактора VIII згортання крові
Показання:
Профілактика та лікування епізодів кровотеч при гемофілії А.
Склад та форма випуску:
Ліофілізат для приготування розчину для внутрішньовенного введення 1 фл.октоког альфа (антигемофільний (рекомбінантний) фактор зсідання крові VIII) 250 МО; 500 МО; 1000 МО
Допоміжні речовини:
Гістидин, гліцин, натрію хлорид, кальцію хлорид, полісорбат 80у флаконах (у комплекті з 2,5 мл розчинника (вода для ін'єкцій) у шприці, адаптером для флакона, пристроєм для внутрішньовенного введення); у пачці картонної 1 комплект
Опис лікарської форми:
Ліофілізат: білий з жовтуватим відтінком порошок.
Приготовлений розчин:
Прозора рідина від безбарвного до жовтого кольору.
Характеристика:
Когенейт ФС є стерильний, стабільний, очищений, непірогенний висушений концентрат, виготовлений з використанням технології рекомбінантних ДНК.
Фармакологічна дія:
Гемостатичний препарат є високоочищеним глікопротеїном, що складається з декількох пептидів, включаючи один з молекулярною масою 80 кД і різні розширені субодиниці з молекулярною масою 90 кД. Виготовлений із використанням технології рекомбінантних ДНК. Виробляється клітинами нирок дитинчат хом'ячків (ВНК), до яких було введено ген людського фактора згортання крові VIII (FVIII). Середовище клітинної культури містить розчин білків плазми людини (HPPS) та рекомбінантний інсулін, але не містить білків, отриманих із тваринних джерел. Когенейт ФС має таку ж біологічну активність, як і фактор VIII, що отримується з плазми крові людини.
Процес очищення включає етап вірусної інактивації ефективним розчинником/детергентом на додаток до класичних методів очищення за допомогою іонообмінної хроматографії, імуноафінної хроматографії з моноклональними антитілами, поряд з іншими хроматографічними етапами, призначеними для очищення рекомбінантного фактора.
Крім того, виробничий процес досліджувався щодо його здатності знижувати інфективність експериментального агента трансмісійної губчастої енцефалопатії (ТГЕ), який розглядався як модель агентів БКЯ (хвороби Крейтцфельда-Якоба) та варіанта БКЯ. Було показано, що ряд окремих етапів виробництва та підготовки вихідної сировини у процесі виготовлення Когенейту ФС знижує ефективність цієї експериментальної моделі агента. Етапи скорочення інфективності ТГЕ включали етап поділу фракції II + III у розчині білків плазми людини (6.0 log10) та етап аніонообмінної хроматографії (3.6 log10). Дані дослідження дають обґрунтовану гарантію того, що у разі наявності у вихідному матеріалі збудника БКЯ/варіанту БКЯ з низьким ступенем інфективності вона може бути усунена.
Введення Когенейту ФС забезпечує збільшення вмісту фактора VIII у плазмі крові та тимчасово усуває дефект коагуляції у хворих на гемофілію А (спадкова кровоточивість, що характеризується недостатньою активністю специфічного білка плазми, VIII фактора згортання крові).
У кожному флаконі Когенейта ФС міститься вказана на етикетці кількість рекомбінантного фактора VIII у міжнародних одиницях (ME). Згідно з встановленим стандартом ВООЗ для фактора згортання крові людини VIII, 1 ME приблизно дорівнює рівню активності фактора VIII в 1 мл пулу свіжої плазми людини.
Фармакокінетика:
Середнє відновлення активності фактора VIII виміряне через 10 хв після інфузії Когенейта ФС склало 2.1±0.3%/МЕ/кг. Середній біологічний T1/2 рекомбінантного фактора VIII (rFVIII-FS), що містить сахарозу, становив приблизно 13 годин і був схожий на T1/2 антигемофільного фактора (АГФ), що отримується з плазми крові людини. Когенейт ФС вкорочував АЧТБ. Відновлення активності фактора rFVIII-FS та його T1/2 не змінювалися через 24 тижні лікування тільки цим препаратом, що вказує на збереження ефективності та відсутність формування антитіл до фактора VIII. Середнє відновлення активності фактора VIII, виміряне через 10 хв після введення дози rFVIII-FS 37 пацієнтам (через 24 тижні лікування rFVIII-FS), склало 2.1%/МЕ/кг, що не відрізнялося від показника відновлення активності фактора VIII, який визначався на вихідному рівні, а також через 4 та 12 тижнів лікування.
Дозування:
Зазначені дози є орієнтовними. Дозу Когенейту ФС, необхідну відновлення гемостазу, слід підбирати індивідуально, залежно від інтенсивності кровотечі, наявності інгібіторів і бажаного рівня чинника VIII. У процесі лікування може знадобитися контроль вмісту фактора VIII. Клінічний ефект фактора VIII є найважливішим в оцінці ефективності лікування. Для досягнення задовільного клінічного результату може знадобитися введення більшої дози фактора VIII, ніж було розраховано. Якщо після введення розрахованої дози не вдається забезпечити очікувану концентрацію фактора VIII або контролювати кровотечу, слід припустити присутність у хворого в крові інгібітора до фактора VIII. Його наявність та кількість (титр) має бути підтверджено відповідними лабораторними тестами. За наявності інгібітору доза фактора VIII у різних пацієнтів може суттєво варіювати, і оптимальна схема лікування визначається лише з урахуванням клінічної відповіді.
Деяких пацієнтів з низьким титром інгібіторів (<10 одиниць Бетезда) можна успішно лікувати препаратами фактора VIII без підвищення анамнестичного титру інгібіторів. Для забезпечення адекватної відповіді необхідно перевіряти рівень фактора VIII та клінічну відповідь на лікування. Пацієнтам з анамнетичною відповіддю на лікування фактором VIII та/або з вищими титрами інгібіторів може знадобитися використання альтернативних лікарських засобів, таких як концентрати комплексу фактора IX, антигемофільний фактор (свинячий), рекомбінантний фактор VIIa або антиінгібіторний комплекс згортання крові.
Процентне підвищення рівня фактора VIII in vivo можна розрахувати за такою формулою: доза Когенейту ФС у МО/кг маси тіла х 2%/МЕ/кг. Цей метод розрахунку заснований на клінічних даних про застосування отриманих із плазми та рекомбінантних продуктів АГФ та ілюструється на наступних прикладах:
Очікуваний % підвищення фактора VIII = (у введених одиниць х 2%/МО/кг)/маса тіла (кг).
Приклад розрахунку дози для дорослого з масою тіла 70 кг: (1400 МО х 2%/МО/кг)/70 кг = 40%.
Необхідна доза (MО) = (маса тіла (кг) х бажаний % підвищення фактора VIII)/2%/МО/кг.
Приклад розрахунку дози для дитини вагою 15 кг (15 кг х 100%)/2%/МО/кг = потрібно 750 MО.
Доза, необхідна для досягнення повноцінного гемостазу, визначається типом та тяжкістю геморагічного епізоду, можете ознайомитись тут
Концентрати АГФ можна також регулярно вводити з метою профілактики кровотеч.
Препарат вводять тільки шляхом внутрішньовенної ін'єкції або інфузії. Після приготування розчин повинен бути введений протягом 3 год. Для введення рекомендується використовувати систему, що додається.
Швидкість введення визначається відповідно до індивідуальної реакції хворого. Як правило, введення всієї дози протягом 5-10 хв і навіть швидше переноситься добре.
Правила приготування розчину Когенейт ФС:
Приготування препарату, його введення та всі маніпуляції із системою для введення слід виконувати дуже уважно. Когенейт ФС з адаптером для флакона є безигольною системою, яка дозволяє попереджати травми в результаті уколів голкою під час приготування розчину. При пошкодженні шкіри голкою, забрудненою кров'ю, можуть передаватися віруси різних інфекцій, зокрема ВІЛ (СНІД) та гепатиту. У разі травми слід негайно звернутися за медичною допомогою. Голки слід поміщати в контейнери, що додаються, відразу ж після використання, всі пристосування для приготування та введення препарату, включаючи залишки приготовленого розчину Когенейту ФС, слід викидати у відповідний контейнер.
- Ретельно вимити руки теплою водою із милом.
- Зігріти в руках закритий флакон і шприц до кімнатної температури (не вище 37 ° С).
- Видалити з флакона захисний ковпачок. Продезінфікувати спиртом гумову пробку, намагаючись не торкатися гумової пробки руками.
- Поставити флакон із препаратом на тверду не слизьку поверхню. Зняти паперове покриття із пластикового картриджа адаптера для флакона. Не виймати адаптер із пластикового картриджа. Взяти картридж із адаптером, помістити його на флакон із препаратом та сильно притиснути. Адаптер зафіксується на кришці флакона.Не знімайте картридж із адаптера на цьому етапі.
- Обережно відкрити блістерне пакування шприца, відігнувши до середини паперове покриття. Вийняти попередньо заповнений шприц із розчинником. Взявши стрижень поршня за верхню насадку, дістати з упаковки. Не слід торкатися сторін та різьблення стрижня поршня. Тримаючи шприц прямо, взяти поршень за верхню насадку і приєднати стрижень, щільно вкрутивши його за годинниковою стрілкою в пробку з різьбленням.
- Взявши шприц за корпус, відламати кришку з кінчика шприца. Необхідно стежити за тим, щоб кінчик шприца не стикався з рукою або будь-якою іншою поверхнею. Відкласти шприц до наступної маніпуляції.
- Зняти картридж адаптера та викинути його.
- Приєднати попередньо заповнений шприц, повертаючи його за годинниковою стрілкою, до нарізного адаптера флакона.
- Ввести розчинник, повільно натискаючи на стрижень поршня.
- Обережно обертати флакон, доки вся речовина не розчиниться. Чи не струшувати флакон. Слід переконатися, що порошок повністю розчинився. Не використовувати розчин, якщо він каламутний або містить видимі частинки.
- Набрати розчин у шприц, утримуючи флакон за край над адаптером флакона та шприцом, а потім повільно та плавно відтягнути стрижень поршня. Необхідно переконатися, що весь вміст флакона набрано в шприц.
- Не змінюючи положення поршня, вийміть шприц із адаптера флакона (останній повинен залишатися приєднаним до флакона). Приєднати шприц до системи, що додається, для введення препарату і ввести розчин внутрішньовенно. Необхідно слідувати інструкції з використання інфузійної системи, що додається.
- Якщо хворому потрібно ввести більше одного флакона, то слід приготувати розчин у кожному флаконі за допомогою шприца, що додається, з розчинником, а потім з'єднати розчини у більшому шприці (не додається) і ввести препарат у звичайному порядку.
- Лікарські засоби для парентерального введення перед введенням слід уважно оглянути наявність сторонніх частинок або зміну кольору, якщо це дозволяють розчин і контейнер.
Передозування:
Симптоми передозування Когенейт ФС невідомі.
Лікарська взаємодія:
Лікарська взаємодія препарату Когенейт ФС не вивчена.
Вагітність та лактація:
Немає даних про застосування препарату Когенейт ФС при вагітності. Невідомо, чи може препарат викликати ушкодження плода чи впливати на репродуктивну здатність при введенні вагітної жінки.
Застосування препарату при вагітності та в період лактації можливе лише за наявності абсолютних показань.
Експериментальні дослідження впливу Когенейт ФС на репродуктивні функції тварин не проводилися.
Побічна дія:
З боку центральної нервової системи: у поодиноких випадках – запаморочення, деперсоналізація.
Дерматологічні реакції: у поодиноких випадках – висипання, свербіж.
З боку травної системи: у поодиноких випадках – незвичайний смак у роті, нудота.
Інші: у поодиноких випадках – помірне підвищення артеріального тиску, риніт, реакції у місці введення.
Умови та термін зберігання:
Препарат слід зберігати у недоступному для дітей, захищеному від світла місці при температурі від 2° до 8°С; не заморожувати. Термін придатності ліофілізату – 30 міс, розчинника – 48 міс.
Дозволяється зберігати препарат при температурі не вище 25°С не більше 3 місяців, наприклад, при лікуванні в домашніх умовах.
Протипоказання:
- Підвищена чутливість до компонентів препарату;
- Підвищена чутливість до білків мишей чи хом'ячків.
Особливі вказівки:
У літературі описані випадки артеріальної гіпотензії, кропив'янки та сором у грудній клітці у зв'язку з реакціями підвищеної чутливості у пацієнтів, які отримували лікування концентратами антигемофільного фактора. При розвитку серйозних анафілактичних реакцій потрібне негайне екстрене лікування із застосуванням реанімаційних заходів, таких як введення епінефрину та кисню.
Когенейт ФС призначений на лікування епізодів кровотечі, обумовлених дефіцитом чинника VIII. Наявність цього дефіциту має бути встановлена до введення Когенейту ФС.
Когенейт ФС не містить фактора Віллебранда, тому не показаний для лікування хвороби Віллебранду.
Під час лікування хворих на гемофілію А можливе утворення циркулюючих нейтралізуючих антитіл (інгібіторів) до фактора VIII. Інгібітори особливо часто з'являються в перші роки лікування у дітей раннього віку, які страждають на тяжку форму гемофілії, або у тих хворих, які раніше отримали обмежену кількість фактора VIII. Однак поява інгібіторів можлива у будь-який момент у процесі лікування пацієнта з гемофілією А. Хворі, які отримують лікування будь-яким препаратом АГФ, у т.ч. Когенейтом ФС, потребують ретельного моніторингу з метою виявлення антитіл до фактора VIII за допомогою належного клінічного спостереження та лабораторних досліджень відповідно до рекомендацій Центру з лікування хворих на гемофілію. Протягом клінічних досліджень за участю пацієнтів, які попередньо отримували лікування, було зареєстровано 109 небажаних явищ на 4160 інфузій (2.6%). Наявність принаймні віддаленого зв'язку з досліджуваним препаратом відзначалося дослідником лише у 13 з цих явищ. Ще 7 небажаних явищ не оцінювали. Таким чином, 20 небажаних явищ у 11 пацієнтів розглядалися або як такі, що не піддаються оцінці, або як принаймні віддалено пов'язані із застосуванням Когенейту ФС з частотою 0.5% щодо кількості вироблених інфузій. У 72 попередньо лікованих пацієнтів з тяжкою формою гемофілії А, які отримували Когенейт ФС, в середньому протягом 54 днів інгібіторів фактора VIII не виявлялося.
У ході клінічних досліджень у всіх пацієнтів проводилися аналізи щодо виявлення сероконверсії щодо білків мишей і хом'ячків. Після початку лікування специфічних антитіл до цих білків не виробилося жодного з пацієнтів, і жодних серйозних алергічних реакцій, пов'язаних з тваринними білками, на тлі інфузій rFVIII - FS не відзначалося. Незважаючи на це, пацієнти повинні бути поінформовані про можливість розвитку реакції підвищеної чутливості до білків мишей та/або хом'ячків та попереджені про ранні ознаки такої реакції (наприклад, кропив'янка, локалізована або генералізована кропив'янка, свистяче дихання та артеріальна гіпотензія). Пацієнтам слід рекомендувати при появі таких симптомів припинити використання препарату і звернутися до свого лікаря.
Клінічні дослідження Когенейта ФС не включали достатньої кількості пацієнтів віком 65 років і старше, щоб можна було визначити, чи відрізняється їхня відповідь на лікування від відповіді молодших пацієнтів. Як і для будь-яких пацієнтів, які отримують Когенейт ФС, дозу для пацієнтів похилого віку потрібно підбирати індивідуально.
Використання в педіатрії:
Когенейт ФС можна використовуватиме лікування дітей. Дослідження безпеки та ефективності проводилися у дітей (n = 62), які попередньо не отримували лікування та отримували мінімальне лікування.
Вплив на здатність до керування автотранспортом та управління механізмами:
Немає відомостей, що введення препарату Когенейт ФС може зменшити здатність керувати автомобілем або працювати з машинами.
Результати експериментальних досліджень:
Проведений in vitro аналіз мутагенного потенціалу rFVIII у дозах, що значно перевищують максимальну терапевтичну дозу, не виявив зворотної мутації або хромосомних аберацій. Дослідження rFVIII in vivo на тваринах з використанням доз, що в 10-40 разів перевищують очікуваний терапевтичний максимум, також показало, що rFVIII не має мутагенного потенціалу. Довгострокових досліджень щодо канцерогенного потенціалу у тварин не проводилося.