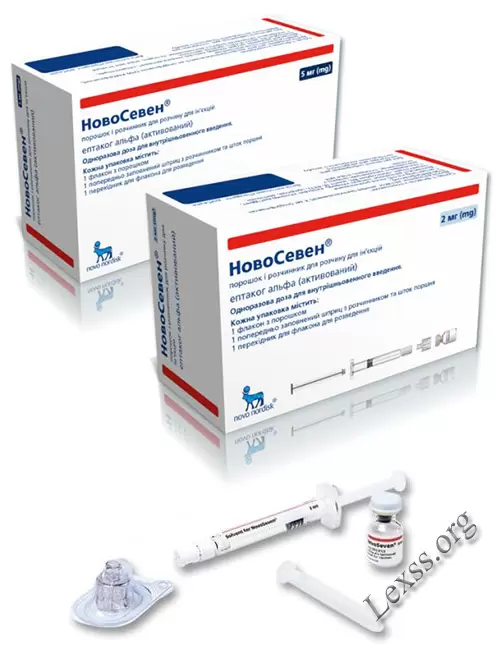
НовоСевен (NovoSeven) - Фактор згортання крові
Міжнародна непатентована назва:
Ептаког альфа (активований): рекомбінантний коагуляційний фактор VIIa.
Виробник:
Ново Нордіск А/О Ново Алле DK-2880 Багсваєрд Данія
Лікарська форма:
Ліофілізат для приготування розчину для внутрішньовенного введення.
Опис:
Білий гомогенний ліофілізат.
Фармакотерапевтична група:
Гемостатичний засіб.
Фармакологічні властивості:
Ептаког альфа (активований) є рекомбінантним фактором згортання VIIа з молекулярною масою, що дорівнює приблизно 50000 дальтон, одержуваний методом генної інженерії з клітин нирок хом'ячків (BHK-клітини).
НовоСевен містить активований рекомбінантний фактор згортання VII.
Механізм дії препарату полягає у зв'язуванні фактора VIIа з тканинним фактором, що вивільнився. Комплекс, що утворився, активує фактор IX з утворенням активного фактора IXа і фактор X з утворенням активного фактора Xa, що призводить до первинного перетворення невеликої кількості протромбіну на тромбін. Тромбін активує тромбоцити та фактори V та VIII у зоні пошкодження та шляхом перетворення фібриногену на фібрин забезпечує утворення гемостатичної пробки.
У фармакологічних дозах препарат НовоСевен безпосередньо, незалежно від фактора тканини, активує фактор X на поверхні активованих тромбоцитів, локалізованих у зоні пошкодження. Це призводить до утворення протромбіну тромбіну у великій кількості незалежно від тканинного фактора. Таким чином, фармакодинамічний ефект фактора VIIа полягає у посиленій місцевій освіті фактора Xa, тромбіну та фібрину. Теоретично не можна повністю виключити ризик системної активації згортання крові у хворих, які страждають на захворювання, що привертають до розвитку ДВС-синдрому.
Фармакокінетичні властивості:
Інгібіторна гемофілія А та В:
Використовуючи коагуляційний метод визначення активності фактора VII, фармакокінетичні властивості препарату НовоСевен вивчали у 25 випадках поза умов кровотечі та у 5 випадках кровотечі.
Було проаналізовано коагуляційну активність фактора VII у плазмі крові до та протягом 24 годин після введення препарату НовоСевен. Фармакокінетика препарату НовоСевен при одноразовому введенні в дозі 17,5, 35 та 70 мкг на кг маси тіла мала лінійний характер. Середні здається обсяги розподілу у стійкому стані і у фазі виведення склали 106 і 122 мл/кг в умовах поза кровотечі і 103 і 121 мл/кг при кровотечі. Середній кліренс у двох групах становив 31,0 мл/годину х кг та 32,6 мл/годину х кг, відповідно. Виведення препарату було описано за допомогою середнього часу перебування в плазмі крові та періоду напіввиведення, які відповідно склали 3,44 години та 2,89 години (середні показники) для умов поза кровотечі та 2,97 та 2,30 години при кровотечі. Середній показник відновлення плазми становив 45,6% у хворих поза умовами кровотечі та 43,5% у хворих під час кровотечі.
Дефіцит фактора VII:
Фармакокінетика препарату
НовоСевен при одноразовому введенні в дозі 15 і 30 мкг на кг маси тіла не мала суттєвих відмінностей за дозо-незалежними параметрами загального кліренсу (70,8-79,1 мл/годину х кг), обсягом розподілу у стійкому стані (280-290 мл /кг), середньому часу перебування у плазмі (3,75 - 3,80 години) та періоду напіввиведення (2,82 - 3,11 години). Середній показник відновлення плазми in vivo становить приблизно 20%.
Тромбастенія Гланцмана:
Фармакокінетика препаратуНовоСевен у хворих, які страждають на тромбастенію Гланцмана, не вивчалася, але передбачається, що вона подібна до фармакокінетики даного препарату у хворих на гемофілію А і В.
Показання до застосування:
НовоСевен використовується для зупинки кровотеч та попередження кровотеч при проведенні хірургічних втручань та інвазивних процедур у наступних групах хворих:
- У хворих на спадкову гемофілію з титром інгібіторів факторів згортання VIII або IX > 5БЕ
- У хворих на спадкову гемофілію з очікуваною імунною реакцією на введення фактора VIII або фактора IX на підставі анамнезу
- У хворих на набуту гемофілію
- У хворих з уродженим дефіцитом фактора VII
- У хворих на тромбастенію Гланцмана за наявності антитіл до глікопротеїнів IIb-IIIa і рефрактерності (нині або в минулому) до трансфузій тромбоцитарної маси.
Протипоказання:
Відома підвищена чутливість до активного компонента, наповнювачів або білків мишей, хом'ячків або корів може бути протипоказанням до призначення препарату НовоСевен.
Спосіб застосування та дози:
Інгібіторна гемофілія А або В, або набута гемофілія
Показано якомога раніше введення препарату НовоСевен після початку кровотечі. Початкова доза, що рекомендується, вводиться внутрішньовенно струминно, становить 90 мкг на кг маси тіла хворого. Після першої ін'єкції введення препарату НовоСевен можна повторювати. Тривалість лікування та інтервал між введеннями препарату визначаються тяжкістю кровотечі або характером інвазивної процедури/хірургічного втручання
Частота введення препарату:
Кожні 2-3 години до гемостазу. Якщо є показання для продовження лікування після зупинки кровотечі, інтервали між введеннями препарату можуть бути послідовно збільшені до 4, 6, 8 або 12 годин на весь період лікування відповідно до показань.
Кровотечі легкого та середнього ступеня тяжкості (включаючи амбулаторне лікування):
Було показано, що раннє введення препарату в дозі 90 мкг на кг маси тіла в амбулаторних умовах дозволяє ефективно контролювати кровотечі легкої та середньої тяжкості до суглобів, м'язів, шкіри та слизових оболонок. Для забезпечення гемостазу вводили 1-3 дози препарату з 3-годинними інтервалами, для підтримки ефекту призначалася ще одна доза препарату НовоСевен. Тривалість амбулаторного лікування не повинна перевищувати 24 години.
Кровотечі тяжкого ступеня:
Початкова доза препарату, що рекомендується, становить 90 мкг на кг маси тіла і може вводитися на етапі транспортування в клініку, де зазвичай лікується даний пацієнт. Схема подальшої терапії залежить від типу та тяжкості кровотечі. На початку лікування препарат вводиться кожні дві години до клінічного поліпшення. За наявності показань до продовження терапії інтервали між введеннями препарату можуть бути збільшені до 3 годин протягом 1-2 діб. В подальшому інтервали між введеннями препарату можна збільшувати до 4, 6, 8 або 12 годин на весь період лікування відповідно до показань. Тривалість лікування тяжкої кровотечі може становити 2-3 тижні або більше за наявності клінічних показань.
Порушення з боку крові та лімфатичної системи:
Дуже рідко (<1/10000)
Виявлено декілька випадків коагулопатій, таких як підвищення рівня Д-димеру та коагулопатії накопичення.
Порушення з боку серця:
Дуже рідко (<1/10000).
Інфаркт міокарда: див. нижче у розділі “Серйозні побічні ефекти у клінічній практиці”.
Шлунково-кишкові розлади:
Дуже рідко (1/10000, <1/1000).
Описано випадки недостатньої ефективності (зниження терапевтичної дії). Необхідно, щоб схема призначення препарату НовоСевен відповідала рекомендованим режимам, описаним у розділі «Дозування».
Дуже рідко (<1/10000)
Можлива лихоманка. Також у дуже поодиноких випадках відзначається біль (особливо у місці ін'єкції).
Зміни лабораторних показників:
Дуже рідко (<1/10000)
Зареєстровані випадки підвищення рівня аланінамінотрансферази, лужної фосфатази, лактатдегідрогенази та протромбіну.
Порушення з боку нервової системи:
Дуже рідко (<1/10000).
Описано випадки цереброваскулярних порушень, у тому числі інфаркту мозку та ішемії мозку: див. нижче у розділі «Серйозні побічні ефекти у клінічній практиці»
Шкірні реакції та порушення з боку підшкірної клітковини:
Можлива поява шкірного висипу
Судинні порушення:
Дуже рідко (<1/10000)
Описані випадки тромбозу вен: див. нижче у розділі “Серйозні побічні ефекти у клінічній практиці” Описані випадки кровотечі на фоні застосування препарату НовоСевен. Передбачається, що НовоСевен не є причиною кровотечі, проте кровотеча, що вже виникла, може продовжуватися у разі недостатньої ефективності або неправильного дозування препарату.
На постмаркетинговому етапі було зареєстровано такі серйозні побічні ефекти:
- Артеріальний тромбоз: інфаркт або ішемія міокарда, цереброваскулярна патологія та інфаркт кишечника. У переважній більшості випадків хворі на ці ускладнення мали схильність до розвитку артеріального тромбозу (супутнє захворювання, вік, атеросклероз або інші порушення, описані в розділі «Спеціальні попередження та особливі запобіжні заходи»).
- Венозний тромбоз: тромбофлебіт, тромбоз глибоких вен та їх ускладнення – тромбоемболії легеневої артерії. У переважній більшості випадків ці хворі мали схильність до розвитку венозного тромбозу через наявність супутніх факторів ризику. Хворі, у яких існує ризик розвитку венозного тромбозу, обумовлений супутніми захворюваннями, наявністю тромбозу в анамнезі, іммобілізацією в післяопераційному періоді або катетеризацією вени, потребують ретельного спостереження. Алергологічний анамнез потребують ретельного спостереження. Антитіл до фактора VII у хворих на гемофілію А і В виявлено не було. Описано окремі випадки появи антитіл до фактору VII після застосування препарату НовоСевен у хворих із дефіцитом фактора VII. Цим хворим раніше переливали людську плазму та/або плазматичний фактор VII. У двох хворих було виявлено інгібуючий ефект антитіл in vitro. У хворих із дефіцитом фактора VII слід проводити контроль на антитіла до фактору VII. Описано один випадок ангіоневротичного набряку у хворого, який страждає на тромбастенію Гланцмана, після введення препарату НовоСевен.
Передозування:
У літнього пацієнта (старше 80 років) чоловічої статі, що страждає на дефіцит фактора VII, що отримав препарат у дозі, що перевищувала рекомендовану дозу в 10-20 разів спостерігалося тромботичне ускладнення Інших тромботичних ускладнень від передозування не спостерігалося, в тому числі, після лікування 6- , що страждає на гемофілію А з інгібіторами, який отримав препарат у дозі, що перевищувала рекомендовану дозу в 8-10 разів.
Взаємодія з іншими лікарськими засобами та інші види взаємодії:
Дані про ризик можливої взаємодії між препаратом НовоСевен та концентратами факторів згортання відсутні. Не слід одночасно вводити концентрати протромбінового комплексу (активовані або неактивовані) та НовоСевен За наявними даними, антифібринолітики знижують інтраопераційну крововтрату у хворих на гемофілію, особливо при ортопедичних операціях та операціях на тканинах з високою фібринолітичною активністю, наприклад: у порожнині рота. Досвід комбінованого застосування антифібринолітиків та препарату НовоСевен обмежений.
Особливі вказівки та запобіжні заходи:
Моніторинг у процесі лікування – лабораторні дослідження:
Терапія препаратом НовоСевен не потребує лабораторного контролю. Дози препарату визначаються залежно від тяжкості кровотечі та клінічного ефекту. Було показано, що після введення препарату НовоСевен протромбіновий час (ПВ) та активований парціальний тромбопластиновий час (АПТВ) знижуються, проте кореляції між ПВ та АПТВ та клінічною ефективністю препарату НовоСевен виявлено не було.
При патологічних станах, що супроводжуються підвищеним вивільненням тканинного фактора, застосування препарату НовоСевен може бути пов'язане з потенційним ризиком розвитку тромботичних ускладнень або синдрому дисемінованого внутрішньосудинного згортання (ДВЗ). Оскільки рекомбінантний фактор згортання VIIа - препарат НовоСевен - може містити слідові кількості мишачого IgG, коров'ячого IgG та інші залишкові білки культури (сироваткові білки хом'ячків та корів), у хворих, які отримують даний препарат, існує дуже мала можливість розвитку підвищеної чутливості до цих білків. При тяжких кровотечах препарат бажано використовувати в клініках, що спеціалізуються на лікуванні гемофілії з інгібіторами до факторів згортання VIII або IX, а, якщо це неможливо, у тісній співпраці з лікарем, що спеціалізується на лікуванні гемофілії. Якщо цей час не вдається зупинити кровотечу, обов'язкова госпіталізація хворого. Пацієнти або особи, які здійснюють догляд за ними, повинні, за першої ж можливості, повідомляти лікаря або клініку про кожен випадок застосування препарату НовоСевен в домашніх умовах. У хворих з дефіцитом фактора VII слід контролювати протромбіновий час та активність фактора VII до та після введення препарату НовоСевен. Якщо активність фактора VIIa не досягає очікуваного рівня або кровотеча продовжується, незважаючи на застосування препарату в дозах, що рекомендуються, можна припустити утворення антитіл. У цьому випадку слід здійснити аналіз на наявність антитіл. Дані щодо ризику тромбозу у хворих з дефіцитом фактора VII на фоні лікування препаратом НовоСевен відсутні. Невикористані продукти та відходи слід знищувати відповідно до місцевих вимог.
Використання під час вагітності та годування груддю:
Як показали досліди на тваринах, внутрішньовенне введення препарату НовоСевен не впливає на розвиток плода, фертильність та репродуктивні властивості. Невідомо, чи здатний НовоСевен при введенні вагітній жінці викликати ушкодження плода або призводити до порушення репродуктивної функції. Застосування препарату НовоСевен у вагітних жінок слід обмежити суворими показаннями. Використання під час годування груддю: не відомо, чи виділяється НовоСевен із грудним молоком. Слід бути обережними при призначенні препарату НовоСевен матерям-годувальницям.
Вплив на здатність до керування автомобілем та обслуговування машин:
Невідомо.
Форма випуску:
Ліофілізат для приготування розчину для внутрішньовенного введення 1,2 мг (60 КЕД); 2,4 мг (120 КЕД) або 4,8 мг (240 КЕД) у флаконі з безбарвного скла, закупореному пробкою з бромбутилової ліофілізаційної гуми, алюмінієвим ковпачком і пластмасовою кришкою «Snap-off», в комплекті з розчинником (вода) у флаконі з безбарвного скла, закупореному пробкою з бромбутилової гуми з тефлоновим покриттям зсередини, алюмінієвим ковпачком та пластмасовою кришкою Snap-off, стерильним адаптером для флакона (для розведення); стерильним одноразовим поліпропіленовим шприцом для розведення та введення; стерильною системою для переливання; двох спиртових тампонів для обробки гумових пробок на флаконах; інструкцією із застосування в коробці з картону.
Умови зберігання:
Зберігати при температурі від 2 до 8°С (у холодильнику).
Зберігати в оригінальній упаковці для захисту від дії світла.
Чи не заморожувати, щоб не пошкодити флакон з розчинником.
Зберігати у недоступному для дітей місці.
Термін придатності:
Термін придатності препарату у комерційній упаковці становить 3 роки.
Було показано, що при температурі 25°С препарат зберігає хімічні та фізичні властивості протягом 24 годин після розведення. З мікробіологічної точки зору препарат слід використовувати відразу після розведення. У тому випадку, якщо весь розведений препарат вводиться не відразу, відповідальність за тривалість та умови зберігання (як правило, це не більше 24 годин при температурі від 2°С до 8°С), несе користувач, за винятком випадків розведення препарату у контрольованих, асептичні умови, підтверджені в установленому порядку. Не використовувати після закінчення терміну придатності.