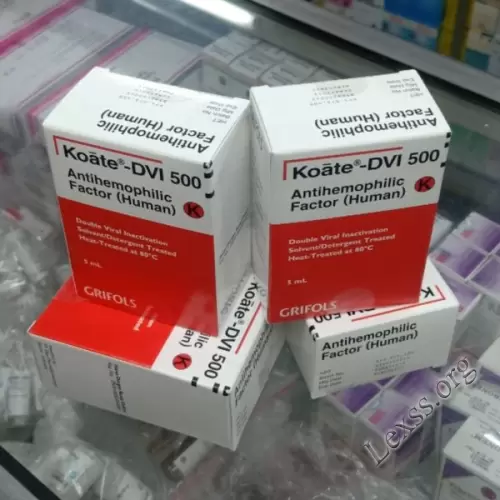
Коейт-ДВІ (Koate-DVI) - фактор згортання крові VIII
Виробники:
Байєр АГ (Сполучені Штати Америки), Талекріс Біотерапьютікс Інк (Сполучені Штати Америки)
Діяча речовина:
Чинник згортання крові VIII (Coagulation Factor VIII) (Coagulation Factor VIII)
Опис лікарської форми:
Ліофілізат для приготування розчину для внутрішньовенного введення - біла або світло-жовта аморфна маса.
Характеристика:
Коейт-ДВІ - концентрат фактора згортання крові VIII, приготований з людської плазми, двічі вірусінактивованої (обробка гарячою парою та сольвент-детергентна обробка).
Склад та форма випуску:
Ліофілізат для приготування розчину для внутрішньовенного введення 200–399 МО 1 фл.
Високоочищений сухий концентрат людського антигемофільного фактора (АГФ, VIII) 200–399 МО*
Допоміжні речовини: альбумін людини (25 мг), натрію хлорид, L-гістидин, кальцію хлоридрозчинник: вода для ін'єкцій - 5 мл
У флаконах (у комплекті з розчинником (фл.), двосторонньою голкою, голкою-фільтром та набором для вливання); у пачці картонної 1 комплект.
Ліофілізат для приготування розчину для внутрішньовенного введення 400-799 МО 1 фл.
Високоочищений сухий концентрат людського антигемофільного фактора (АГФ, фактор VIII) 400–799 МО*
Допоміжні речовини: альбумін людини (25 мг), натрію хлорид, L-гістидин, кальцію хлорид
Розчинник: вода для ін'єкцій - 5 мл
У флаконах (у комплекті з розчинником (фл.), двосторонньою голкою, голкою-фільтром та набором для вливання); у пачці картонної 1 комплект.
Ліофілізат для приготування розчину для внутрішньовенного введення 800-1400 МО 1 фл.
Високоочищений сухий концентрат людського антигемофільного фактора (АГФ, фактор VIII) 800–1400 МО*
Допоміжні речовини: альбумін людини (50 мг), натрію хлорид, L-гістидин, кальцію хлорид
Розчинник: вода для ін'єкцій - 10 мл
У флаконах (у комплекті з розчинником (фл.), двосторонньою голкою, голкою-фільтром та набором для вливання); у пачці картонної 1 комплект.
*Активність фактора згортання крові VIII (VIII:C) визначалася відповідно до Міжнародного стандарту ВООЗ для концентратів фактора VIII; специфічна активність після додавання альбуміну людського становить 9-22 МО/мг білка.
Фармакологічна дія:
Фармакологічна дія – гемостатична.
Фармакодинаміка:
Механізм дії препарату обумовлений включенням активованого фактора VIII у багатоступінчастий процес згортання крові - зрештою препарат сприяє переходу протромбіну в тромбін та утворенню фібринового згустку.
Застосування препарату забезпечує збільшення вмісту фактора VIII у плазмі крові та тимчасово усуває дефект коагуляції у пацієнтів з гемофілією А.
Коейт-ДВІ містить фактор Віллебранда природного походження.
Фармакокінетика:
Після введення препарату Коейт-ДВІ підвищення активності фактора VIII у плазмі становить від 80 до 120% від очікуваного. У фармакокінетичних дослідженнях відновлення фактора VIII in vivo через 10 хв після введення Коейт-ДВІ в середньому склало 1,9%/кг.
Активність фактора VIII у плазмі крові знижується за двофазною експоненційною кривою. У початковій фазі відбувається його розподіл між внутрішньосудинним руслом та позасудинними тканинними рідинами з T1/2 із плазми 3–6 год; приблизно від 2/3 до 3/4 введеного внутрішньовенного фактора VIII залишається в судинному руслі.
Наступна повільна фаза, можливо, відображає розпад фактора VIII. У цій фазі T1/2 становить від 8 до 20 год, у середньому – 16,12 год. Це відбиває справжній біологічний T1/2 фактора VIII.
Показання:
Лікування та профілактика кровотеч при спадкових (гемофілії A) та набутих дефіцитах фактора згортання крові VIII.
Протипоказання:
Протипоказання. Підвищена чутливість до компонентів препарату.
Застосування при вагітності та годуванні груддю:
Контрольовані дослідження, що підтверджують безпеку застосування концентратів фактора зсідання крові VIII людини при вагітності та лактації, не проводилися. Тому застосування препарату Коейт-ДВІ при вагітності та в період лактації можливе лише за суворими показаннями, коли очікувана користь перевищує можливий ризик для плода, матері або немовляти.
Побічні дії:
Алергічні реакції: в окремих випадках – ангіоневротичний набряк, гіперемія шкіри, кропив'янка, свербіж, озноб, головний біль, артеріальна гіпотензія, сонливість, нудота, блювання, занепокоєння, тахікардія, відчуття здавлення у грудях, стридорозне дихання аж до розвитку анафілакт; рідко – підвищення температури тіла.
При введенні препарату у високих дозах у пацієнтів із групами крові А(II), В(III) або AB(IV) може спостерігатися гемоліз.
Місцеві реакції: в окремих випадках – відчуття печіння у місці ін'єкції.
Передозування:
Симптоми передозування Коейт-ДВІ не відомі.
Спосіб застосування та дози:
В/в, повільно, струминно або краплинно.
Терапія має починатися під наглядом лікаря, який має досвід лікування гемофілії. Дози та тривалість замісної терапії залежать від ступеня дефіциту фактора VIII, локалізації, інтенсивності кровотечі та тяжкості клінічного стану хворого.
Кількість фактора VIII, що вводиться, виражається в Міжнародних одиницях (ME), які відповідають загальноприйнятому стандарту ВООЗ. Активність фактора VIII у плазмі виявляється у відсотках (відповідає нормальній плазмі людини) або у МО (відповідає Міжнародному стандарту для фактора VIII у плазмі). 1 МО активності фактора VIII дорівнює кількості фактора VIII в 1 мл нормальної людської плазми.
Розрахунок дози ґрунтується на емпірично встановленому факті, що при введенні 1 ME фактора VIII на кг маси тіла активність фактора VIII у плазмі підвищується на 1,5–2% нормальної активності.
Необхідна доза препарату Коейт-ДВІ розраховується за такою формулою: доза, MО = (маса тіла, кг × бажане підвищення фактора VIII,%): 2%/МО/кг.
Приклад: дитина масою тіла 15 кг.
Необхідна доза, МО = (15 кг × 100%): 2%/МО/кг = 750 МО.
У кожному конкретному випадку кількість препарату, що вводиться, і частота введення повинні співвідноситися з клінічною ефективністю.
Легкі (несильні поверхневі або ранні) кровотечі можуть припинятись при введенні препарату в дозі 10 МО/кг, що призводить до підвищення рівня фактора VIII приблизно на 20% in vivo. До появи ознак подальшої кровотечі повторного введення не потрібно.
При помірних кровотечах (наприклад, одиночні гемартрози, певні травми) рівень фактора VIII слід піднімати на 30-50% шляхом введення препарату в дозі 15-25 МО/кг. При необхідності продовження терапії повторне введення може здійснюватись у дозі 10–15 МО/кг; препарат слід вводити кожні 8-12 годин до повної зупинки кровотечі.
Для досягнення гемостазу у пацієнтів з тяжкими (загрозливими для життя) кровотечами або кровотечами в життєво важливі органи (наприклад, ЦНС, заковтковий або заочеревинний простір, піхву клубового м'яза) рівень фактора VIII необхідно збільшити на 80-100% від нормального. Цього можна досягти при введенні Коейт-ДВІ з розрахунку 40–50 МО/кг. Підтримуюча доза становить 20-25 МО/кг і вводиться кожні 8-12 годин до повної зупинки кровотечі.
Для здійснення великих хірургічних втручань рівень фактора VIII слід підняти приблизно до 100% шляхом введення передопераційного препарату Коейт-ДВІ у дозі 50 МО/кг. Рівень фактора VIII слід контролювати до і протягом всього операційного періоду для підтвердження адекватності замісної терапії. Для підтримки гемостатичного рівня можуть знадобитися повторні введення кожні 6-12 годин протягом 10-14 днів після операції. Інтенсивність необхідної замісної терапії фактора VIII залежить від типу хірургічного втручання та наступного післяопераційного режиму. Гемостаз для дрібних хірургічних втручань може бути забезпечений менш інтенсивним лікувальним режимом.
Для тривалої профілактики при тяжких формах гемофілії А рекомендується введення препарату в дозі 20–40 МО/кг кожні 2–3 дні. У деяких випадках, особливо у пацієнтів молодшого віку, для профілактики геморагії може знадобитися зменшення інтервалів між введеннями або збільшення доз препарату.
Розчин препарату готується перед введенням. Приготовлений розчин зберігає хімічну та фізичну стабільність протягом 3 годин при температурі 20–25 °C, проте його слід використовувати одразу після приготування. Не можна використовувати каламутний розчин або розчин із включеннями. Невикористаний розчин підлягає відповідній утилізації.
Правила приготування та введення розчину:
Флакони з розчинником та концентратом слід нагріти до кімнатної температури (не вище 37 °C). Після видалення захисних кришок із флаконів слід продезінфікувати гумові пробки обох флаконів. Далі слід видалити захисне покриття у вигляді ізолюючої плівки із пластикового картриджа голки для перенесення та проткнути пробку флакона з розчинником. Видалити частину пластикового картриджа, що залишилася, перевернути флакон з розчинником і проткнути за допомогою голки, розташованої під кутом, гумову пробку флакона з концентратом. Розчинник надійде у флакон із концентратом під дією вакууму. Флакон із розчинником слід тримати під кутом до флакона з концентратом. Після видалення флакона з розчинником та голки слід енергійно обертати флакон з концентратом до повного розчинення порошку, не викликаючи зайвого утворення піни. Після повного розчинення порошку слід набрати розчин у шприц через голку, що додається, з фільтром. Далі слід замінити голку з фільтром на голку для ін'єкцій та ввести розчин внутрішньовенно. Якщо пацієнту потрібно ввести більше одного флакона, вміст двох флаконів може бути набраний в один шприц через різні невикористані голки з фільтром перед приєднанням ін'єкційної голки.
Тривалість введення визначається відповідно до індивідуальної реакції пацієнта і зазвичай становить 5–10 хв.
Умови зберігання препарату Коейт-ДВІ:
У захищеному від світла місці при температурі від 2 до 8 °C (не заморожувати).
Зберігати у недоступному для дітей місці.
Термін придатності препарату Коейт-ДВІ:
24 міс. Після приготування розчину – 3 год.